GH-aksen forklart: GHRH, ghrelin og IGF-1 i samspill
En pilarguide til GH-aksen: hvordan GHRH-analoger og ghrelin-mimetika driver pulsatil veksthormonfrigjøring, og hva somatopausen endrer over tid.
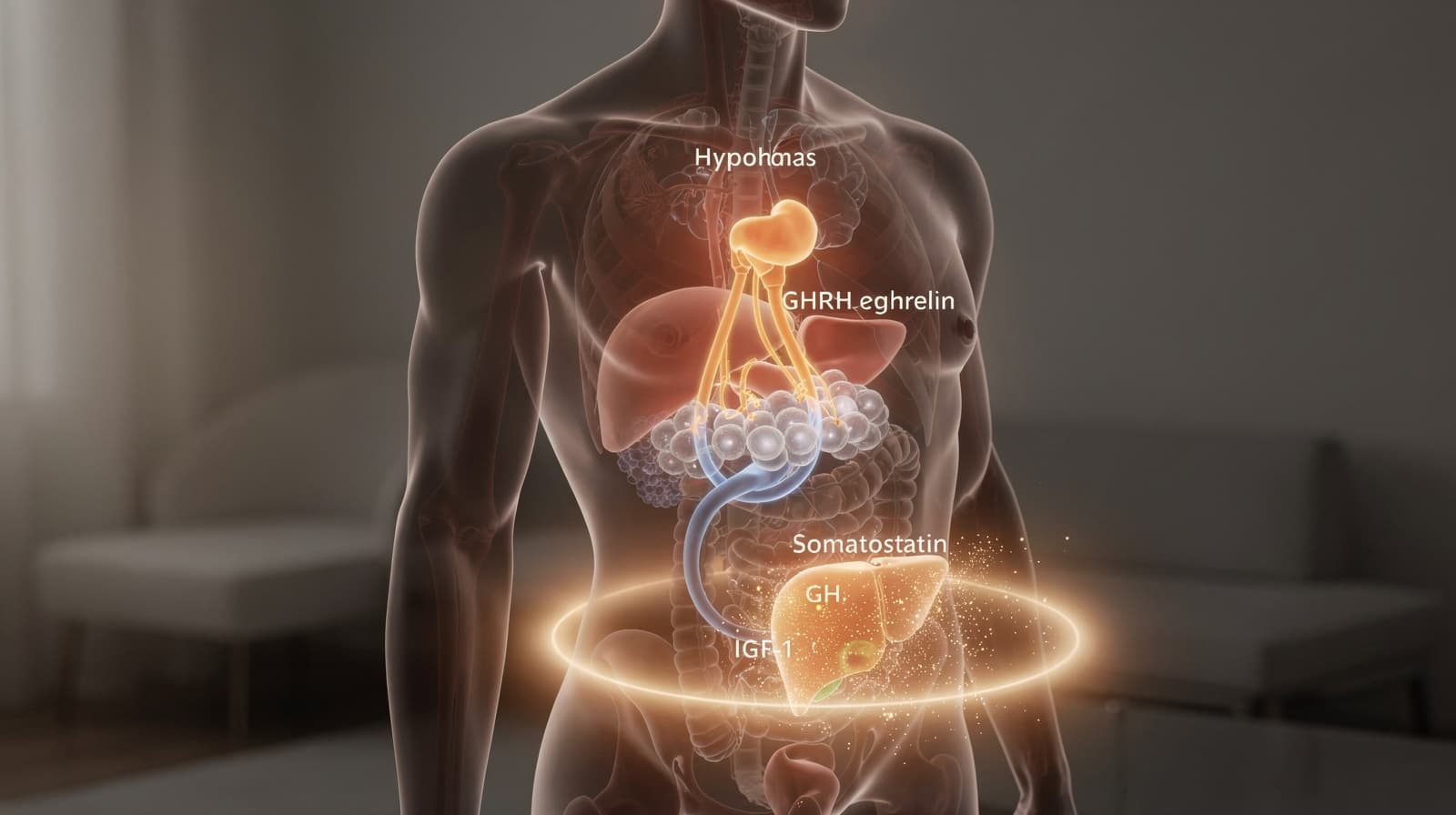
Mye peptidinnhold behandler enkeltmolekyler som frittstående verktøy. Den rammen skjuler en mer nyttig sannhet: ipamorelin, CJC-1295, MK-677 og tesamorelin virker alle på den samme regulatoriske kretsen, og forståelse av denne kretsen forutsier hvilken forbindelse som passer hvilket mål. Denne pilarguiden gjennomgår GH-aksen, reseptorene som er involvert, og hvordan alder endrer bildet.
Hovedpunkter#
- GH-aksen styres av tre innganger: hypothalamisk GHRH (stimulerende), somatostatin (hemmende) og ghrelin fra ventrikkelen (stimulerende via en separat reseptor).
- Somatotrofe celler i hypofysen frigjør veksthormon i pulser; nedstrøms hepatisk IGF-1 lukker tilbakekoblingssløyfen ved å hemme videre GH-utskillelse.
- Forskning antyder at to reseptorfamilier er relevante for peptidprotokoller: GHRH-reseptoren (som CJC-1295 og tesamorelin retter seg mot) og GHSR-1a ghrelin-reseptoren (som ipamorelin og MK-677 retter seg mot).
- Somatopausen, den aldersrelaterte nedgangen i GH og IGF-1, er forbundet med endringer i kroppssammensetning og redusert muskelmasse.
- Kombinasjon av en GHRH-analog med et ghrelin-mimetikum gir en supra-additiv puls, som er den mekanistiske begrunnelsen bak vanlige kombinasjonsprotokoller.
Aksen er en kontrollsløyfe med tre innganger, ikke en enkelt bryter#
Den klassiske beskrivelsen av veksthormonregulering, foredlet siden 1960-tallet, har GHRH og somatostatin som motvirkende hypothalamiske innganger. Hypofysens syntese og sekresjon av GH stimuleres av episodisk hypothalamisk frigjøring av GH-frigjørende faktor og hemmes av somatostatin, mens insulinlignende vekstfaktor 1 (IGF-1) hemmer GH-sekresjon gjennom en negativ sløyfe på både hypothalamisk og hypofysenivå. Store medisinske leksikon beskriver det samme prinsippet: utskillelsen av hormonet skjer i pulser og reguleres fra hypothalamus ved hjelp av GHRH, som er stimulerende, og somatostatin, som er hemmende.
Den tobaserte modellen holdt frem til 1999, da oppdagelsen av ghrelin la til en tredje regulator fra utenfor hjernen. Det gastriske peptidet ghrelin er også en potent GH-sekretagog som virker ved å øke hypothalamisk GHRH-utskillelse og forsterke dens GH-stimulerende effekter i hypofysen. Med andre ord treffer ghrelin en distinkt reseptor (GHSR-1a) og amplifiserer GHRH-signalet både sentralt og i somatotrofen. Norsk metodebok bekrefter at ghrelin produseres i endokrine celler i ventrikkelen og stimulerer til frigjøring av veksthormon fra hypofysen.
Den praktiske implikasjonen: ethvert peptid som påvirker GH-utskillelse må virke gjennom ett av disse tre kontrollpunktene. GHRH-analoger trykker på akseleratoren. Ghrelin-mimetika trykker på en annen akselerator. Ingenting som for tiden er tilgjengelig i forskningspeptidform fjerner somatostatin-bremsen direkte, og det er derfor protokoller tidsbestemmer injeksjoner rundt endogene somatostatin-bunner (vanligvis før søvn eller tidlig morgen i fastet tilstand).
GH-frigjøring er pulsatil, og pulsmønsteret betyr mer enn gjennomsnittet#
Kontinuerlig GH-eksponering reproduserer ikke fysiologien til frisk GH-sekresjon. Studier har vist at GH-sekresjon hos mennesker er pulsatil, og dette mønsteret reguleres av både GHRH og somatostatin, med GH-utbrudd mediert av en reduksjon i tonisk hypothalamisk somatostatin-sekresjon.
Dette er grunnen til at langtidsvirkende rekombinant GH og en velkonstruert peptidprotokoll gir forskjellige nedstrøms signaturer. En kort GHRH-puls lagt på toppen av en endogen somatostatin-bunn bevarer pulsarkitekturen; kontinuerlig reseptoropptak gjør det ikke. Forskning har vist at GH-responsen på vedvarende GHRH-infusjon avtar innen timer, noe som bekrefter at somatostatin-bremsen, ikke GHRH-tilførselen, dikterer pulstiming. Den norske analysebeskrivelsen fra Helse Møre og Romsdal påpeker at den somatotrope aksen har stor fysiologisk betydning for vekst-, differensiering- og stoffskifteprosesser gjennom hele livet.
For protokolldesign følger tre punkter:
- Timing i forhold til måltider er viktig fordi næringsinntak undertrykker GH og hever somatostatin.
- Timing i forhold til søvn er viktig fordi den største endogene GH-pulsen oppstår i tidlig dyp søvn.
- Kombinasjon av en GHRH-analog med et ghrelin-mimetikum er forbundet med en større puls enn noen av forbindelsene alene, fordi de to reseptorene konvergerer på samme somatotrof gjennom komplementær virkning.
To reseptorfamilier, to peptidkategorier#
Hvert peptid markedsført som en "veksthormonsekretagog" faller inn i en av to mekanistiske kategorier, definert av reseptoren det binder seg til.
GHRH-reseptoragonister etterligner endogen GHRH ved GHRH-reseptoren i hypofysen. Veksthormonfrigjørende hormon (GHRH), som skilles ut av nevroner i den arkuate kjernen, stimulerer GH-produksjon i hypofysens forlapp. CJC-1295 og tesamorelin er de to forbindelsene som oftest diskuteres i denne kategorien. Tesamorelin er den eneste FDA-godkjente GHRH-analogen, studert primært ved HIV-assosiert lipodystrofi. Klarovel dekker tesamorelins mekanisme og studiedata i tesamorelin-guiden.
Ghrelin-reseptoragonister (også kalt GHSR-1a-agonister, veksthormonsekretagoger eller "GHS") binder seg til reseptoren som endogen ghrelin aktiverer. Studier viser at ghrelin gir en supra-additiv respons med GHRH i induksjonen av GH-sekresjon; dette er reseptoren som ipamorelin og MK-677 retter seg mot. Ipamorelin er et injisert, korttidsvirkende peptid; MK-677 (ibutamoren) er et oralt biotilgjengelig ikke-peptid ghrelin-mimetikum. Antidoping Norge lister disse forbindelsene blant veksthormonsekretagoger og deres mimetika, inkludert anamorelin, ibutamoren (MK-677), ipamorelin og tesamorelin. Den mekanistiske sammenligningen er beskrevet i MK-677-guiden og ipamorelin-oversikten.
Grunnen til at kombinasjonsprotokoller eksisterer, er nettopp fordi dette er to forskjellige reseptorer med komplementær nedstrøms signalering. Den parede CJC-1295 og ipamorelin-tilnærmingen dekkes i detalj i Klarovels protokollartikkel om CJC-1295 og ipamorelin.
Somatopausen forskyver baselinjen som protokoller forsøker å adressere#
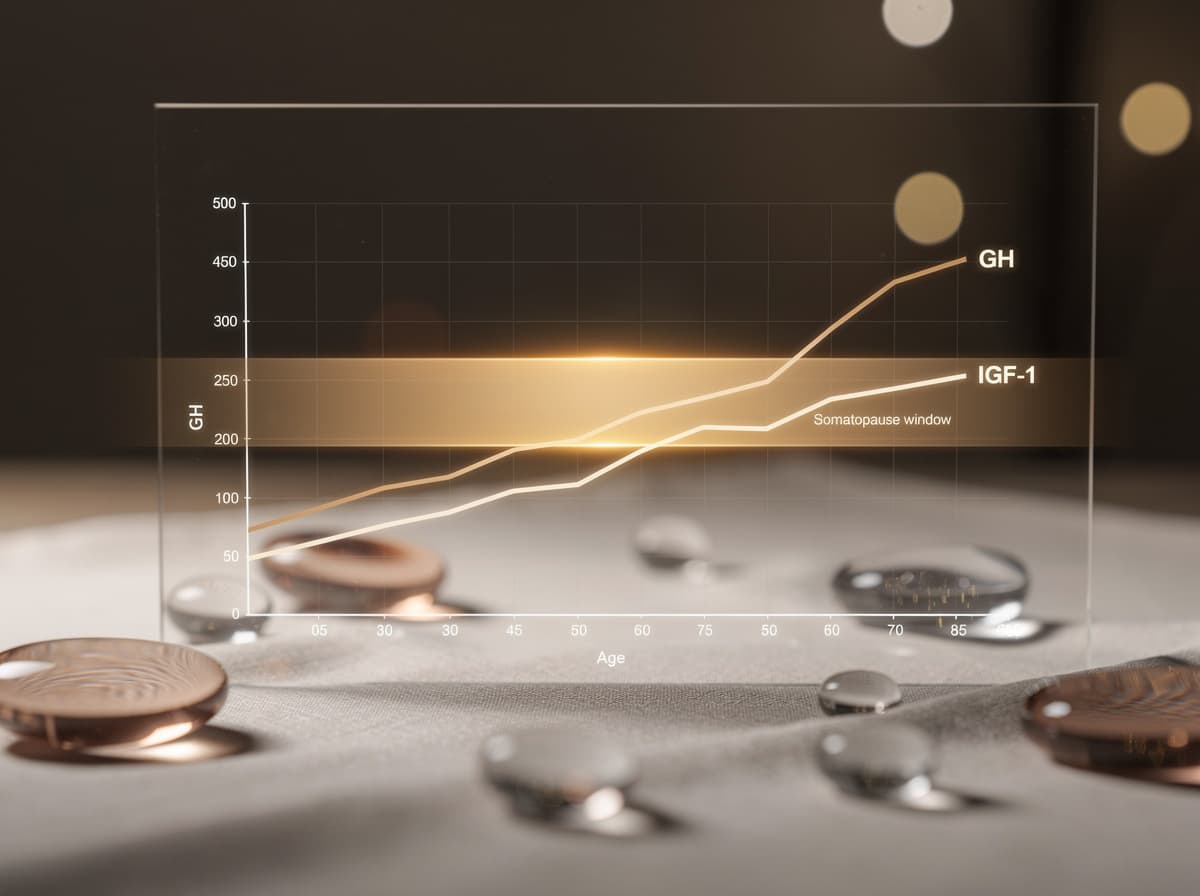
Den biologiske grunnen til at interessen for GH-akse-peptider eksisterer er at aksen svekkes med alderen. Forskning har vist at GH-produksjon og -sekresjon, GH-bindende protein og IGF-1-nivåer synker med alderen, ofte kalt "somatopausen", og at disse reduksjonene danner grunnlaget for spekulasjoner om at disse anabole hormonene er knyttet til endringer i kroppssammensetning, metabolisme og funksjon som oppstår med aldring.
Tallene er sterkere enn folk flest forventer. Etter puberteten synker GH-nivåene eksponentielt; produksjonen rapporteres å avta med 14 % per tiår og kan synke med opptil 50 % hvert syvende år for voksne menn, der eldre menn produserer så lite som 50 μg/dag sammenlignet med gutter i puberteten som produserer 1,0 til 1,5 mg/dag. Studier har vist at den resulterende tilstanden er forbundet med økt fettvev og det bredere settet av endringer som speiler klinisk veksthormonmangel hos voksne. Den norske ressursen fra Antidoping Norge bekrefter at utskillelsen av veksthormon er størst i slutten av tenårene og synker gradvis med økende alder.
En andre klinisk gjennomgang beskriver mekanismen tydelig: aldersrelatert nedgang i GH-nivåer er svært godt dokumentert, konsistent på tvers av ulike pattedyrarter og primært på grunn av redusert hypothalamisk sekresjon av GHRH med påfølgende nedgang i GH-biosyntese og -frigjøring fra hypofysens forlapp, noe som fører til en reduksjon i sirkulerende nivåer av IGF-1, hovedmediatoren for GH-virkning.
To foreløpige funn er viktige for protokolltenkning. For det første er nedgangen oppstrøms: den starter med GHRH, ikke med somatotrof kapasitet, og det er derfor GHRH-analoger forblir effektive hos eldre forsøkspersoner. For det andre dokumenterer tesamorelin-litteraturen at GHRH-agonisten gjenoppretter normal GH-pulsatilitet og amplitude, reduserer selektivt visceralt fett, intima-media-tykkelse og triglyserider, og forbedrer kognitiv funksjon hos eldre personer. Foreløpige funn peker mot å gjenopprette pulsarkitektur, ikke å oversvømme systemet med kontinuerlig GH.
Tilbakekoblingssløyfer og bivirkningsmekanismer kommer fra samme diagram#
Å lese aksen som en sløyfe forklarer også hvorfor noen forbindelser gir spesifikke tolerabilitetsprofiler. Tre tilbakekoblingsnoder er viktige:
- IGF-1 negativ tilbakekobling i hypothalamus. Stigende hepatisk IGF-1 hemmer GHRH-nevroner og stimulerer somatostatin. Dette er grunnen til at kronisk høydose ghrelin-agonisme, spesielt med oral MK-677, kan flate ut over uker: forhøyet IGF-1 lukker sløyfen og demper videre GH-amplitude.
- Ghrelins oreksigene virkning. Den samme reseptoren som driver GH-frigjøring driver også sult. Forskning har vist at ghrelin er et oreksigent hormon som primært frigjøres av magesekkens slimhinne, selv om det er bredt uttrykt i mange forskjellige vev, inkludert sentralnervesystemet og hypofysen. Økt appetitt på MK-677 er ikke en bivirkning; det er on-target farmakologi.
- Insulin- og glukosehåndtering. GH er motregulatorisk mot insulin. Studier viser at under langvarig GH-forhøyelse stiger hepatisk glukoneogenese og frigjøring av frie fettsyrer, noe som kan dempe insulinfølsomhet. Peptidkalkulatoren integrerer dette ved modellering av pulseksponering over en syklus.
Et separat punkt verdt å merke seg: somatostatin hemmer GH-sekresjon og regulerer flere prosesser ved å signalisere gjennom sine reseptorer sst1 til sst5, og differensielt uttrykk av disse reseptorene kan bidra til kjønnsspesifikke GH-mønstre og fasteindusert GH-stigning. Oversettelse: protokollresponser varierer etter kjønn og fôringstilstand, og en enkelt doseringsanbefaling på tvers av populasjoner er sjelden forsvarlig.
Hvordan de fire GH-akse-peptidene plasseres på denne kretsen#
Til sammen opptar de fire peptidene Klarovel dekker i dybden distinkte posisjoner på det samme diagrammet:
- Ipamorelin: korttidsvirkende selektiv GHSR-1a-agonist. Gir en ren GH-puls uten betydelig kortisol- eller prolaktinforhøyelse. Best for brukere som ønsker pulsatil, tidsavgrenset stimulering.
- CJC-1295 (med eller uten DAC): GHRH-reseptoragonist. Uten DAC oppfører den seg som en kort GHRH-puls; med DAC gir den vedvarende GHRH-reseptoreksponering. Ofte paret med ipamorelin for å engasjere begge reseptorer.
- MK-677 (ibutamoren): oralt biotilgjengelig, langtidsvirkende GHSR-1a-agonist. Opprettholder forhøyede 24-timers GH- og IGF-1-gjennomsnitt, men mister pulsarkitektur og engasjerer ghrelin-signalets oreksigene og vannretensjons-effekter mer synlig.
- Tesamorelin: stabilisert GHRH-analog med det tydeligste kliniske evidensgrunnlaget, spesifikt for reduksjon av visceralt fettvev ved HIV-assosiert lipodystrofi i henhold til FDA-merkingen.
For et bredere rammeverk for hvordan disse kandidatene sammenlignes, se hvordan Klarovel strukturerer protokollkurering, og kjør dosevindusscenarier gjennom peptidkalkulatoren. Kontoinnehavere kan lagre protokollmaler via registrering.
Ofte stilte spørsmål om GH-aksen#
Hva er forskjellen på en GHRH-analog og et ghrelin-mimetikum?
De aktiverer ulike reseptorer på de samme cellene i hypofysen. GHRH-analoger (CJC-1295, tesamorelin) binder seg til GHRH-reseptoren; ghrelin-mimetika (ipamorelin, MK-677) binder seg til GHSR-1a. Forskning har vist at de to reseptorene konvergerer på komplementære intracellulære signalveier, og det er derfor kombinasjon av dem gir en større puls enn noen av dem alene.
Hvorfor parer protokoller ofte to peptider i stedet for å bruke ett i høyere dose?
Fordi dose-responskurven ved en enkelt reseptor metter. Den parede tilnærmingen utnytter to uavhengige reseptorer, hver med bidrag til GH-frigjøring. Studier viser at ghrelin gir supra-additiv respons med GHRH, stimulerer GH-sekresjon uavhengig av GHRH-reseptorer, virker både på hypothalamisk og hypofysenivå, og kan funksjonelt motvirke somatostatin. To distinkte mekanismer, ett utfall.
Slutter GH-aksen å fungere med alderen?
Nei, men oppstrøms-signalet svekkes. De somatotrofe cellene i hypofysen forblir i stor grad responsive; det som synker er hypothalamisk GHRH-drift og pulsorganisering. Foreløpige funn antyder at dette er grunnen til at GHRH-analoger som tesamorelin beholder effekt hos eldre forsøkspersoner.
Er somatopausen en sykdom?
Ikke i kliniske termer. Det er en normal aldersrelatert forskyvning. Den er forbundet med endringer i muskelmasse og fettvev som overlapper med voksne GH-mangelfenotyper, men konsensusretningslinjer klassifiserer den ikke som en mangeltilstand som krever intervensjon.
Hvorfor øker MK-677 appetitten når ipamorelin generelt ikke gjør det?
Begge engasjerer GHSR-1a, men farmakokinetikken deres er forskjellig. MK-677 opprettholder reseptoropptak i 24 timer, noe som kontinuerlig engasjerer ghrelins oreksigene sentrale effekter. Ipamorelins korte halveringstid gir en diskret puls som avtar før appetittkretsene aktiveres meningsfullt.
Hvor passer IGF-1 inn i protokolldesign?
IGF-1 er nedstrøms-avlesningen av GH-akse-aktivitet og det negative tilbakekoblingssignalet tilbake til hypothalamus. Sporing av IGF-1 over en syklus gir en nyttig proxy for om en protokoll gir biologisk meningsfull eksponering, samtidig som det signaliserer når den negative tilbakekoblingssløyfen lukkes og pulsamplituden undertrykkes.
Aksesynet endrer hvilke spørsmål som er verdt å stille#
I stedet for å spørre "hvilket peptid er best", omformulerer arbeidskunnskap om GH-aksen spørsmålet: hvilken reseptor, hvilket pulsmønster, hvilket tilbakekoblingsregime passer målet. Den rammen er det Klarovels protokollkurering er bygget rundt. Start med peptidkalkulatoren for å modellere en kandidatprotokoll, gjennomgå det regulatoriske rammeverket i vår opplysningsside, og registrer deg for å lagre arbeidet ditt og følge oppdateringer etter hvert som nye funn kommer.
Les videre
Hva er peptidterapi? Tre kategorier som teller i 2026
Peptidterapi i 2026 betyr tre forskjellige ting: FDA-godkjente legemidler, kompounderte peptider i en gjenåpnet gråsone, og forskningspeptider.

GLP-1-klassen forklart: hvordan semaglutid, tirzepatid og retatrutid skiller seg
Semaglutid, tirzepatid og retatrutid deler samme farmakologifamilie, men aktiverer ulike metabolske reseptorer. Her er hva forskjellen faktisk betyr.
Melanotan 2 Norge: jus, risiko og tryggere brunfarge-veier
Hva forskning viser om Melanotan 2, hvorfor DMP ikke har godkjent peptidet i Norge, publiserte melanom-kasus, og evidensbaserte alternativer for pigmentering.